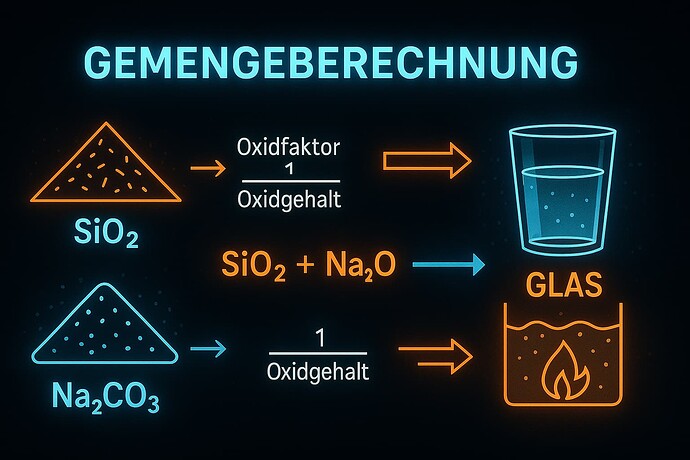
Übersicht: Rohstoffe, Oxide & Reaktionsgleichungen
Übersicht: Rohstoffe, Oxide & Reaktionsgleichungen
Wird für die folgenden Berechnungen benötigt!
| SiO2 | Kein Zerfall – SiO2 bleibt erhalten | |
| Na2O | Na2CO3 → Na2O + CO2 | |
| K2O | K2CO3 → K2O + CO2 | |
| CaO | CaCO3 → CaO + CO2 | |
| CaO + MgO | CaMg(CO3)2 → CaO + MgO + 2 CO2 | |
| Al2O3 | 2 Al(OH)3 → Al2O3 + 3 H2O | |
| Al2O3 | Wird direkt übernommen | |
| B2O3 | 2 H3BO3 → B2O3 + 3 H2O | |
| B2O3 + Na2O | Na2B4O7 → B2O3 + Na2O (vereinfacht) | |
| BaO | BaCO3 → BaO + CO2 | |
| ZnO | ZnO bleibt unverändert | |
| PbO | Pb3O4 → 3 PbO + ½ O2 | |
| As2O3 | Wird direkt übernommen, teilweise flüchtig | |
| – (Läutermittel) | Zersetzt sich, wirkt oxidierend: Na2SO4 → Na2O + SO3 | |
| – (Redoxmittel) | Zersetzt sich zu K2O + NOx + O2 (wirkt stark oxidierend) | |
| – (Redoxmittel) | NaNO3 → Na2O + NOx + O2 (Oxidationsmittel, Entfärberwirkung) | |
| – (Schmelzhilfe) | Bleibt als CaF2 erhalten – wirkt als Flussmittel | |
| SiO2 + Al2O3 + Na2O/K2O | Zerfällt in mehrere Oxidanteile (Netzwerkbildner + Stabilisatoren) |
![]() Hinweise:
Hinweise:
- Reaktionsgleichungen sind thermisch gemeint (bei hohen Temperaturen im Schmelzprozess).
- Läutermittel & Redoxmittel tragen nicht direkt zur Glasmasse bei, beeinflussen aber Farbe & Klarheit.
 Aufgabe 1: Berechne den Gemengesatz für Flachglas
Aufgabe 1: Berechne den Gemengesatz für Flachglas
Ein Flachglas soll folgende Oxid-Zusammensetzung haben (bezogen auf 100 kg Glas):
| Oxid | Anteil [%] |
|---|---|
| SiO2 | 72,01 % |
| Na2O | 15,50 % |
| CaO | 7,60 % |
| MgO | 3,80 % |
| Al2O3 | 0,90 % |
| Fe2O3 | 0,10 % (wird nicht berücksichtigt) |
Verwendete Rohstoffe:
- Quarzsand (für SiO2)
- Soda (Na2CO3 → Na2O)
- Kalk (CaCO3 → CaO)
- Dolomit (CaMg(CO3)2 → MgO + CaO)
- Tonerdehydrat (Al(OH)3 → Al2O3)
Berechne die benötigten Rohstoffmengen und die Glasausbeute.
💡 Lösung anzeigen
 1. SiO₂ aus Quarzsand
1. SiO₂ aus Quarzsand
Rohstoff: Quarzsand
SiO2-Gehalt: 99,5 % → 0,995
 2. Na₂O aus Soda (Na₂CO₃)
2. Na₂O aus Soda (Na₂CO₃)
Reaktionsgleichung:
Na2CO3 → Na2O + CO2
Molmassen:
Na2CO3 = 2×22,99 + 12,01 + 3×16 = 105.99 g/mol
Na2O = 2×22,99 + 16 = 61.98 g/mol
Na2O-Gehalt:
61.98 / 105.99 ≈ 0.585
 3. MgO aus Dolomit (CaMg(CO₃)₂)
3. MgO aus Dolomit (CaMg(CO₃)₂)
Reaktionsgleichung:
CaMg(CO3)2 → CaO + MgO + 2 CO2
Molmasse Dolomit:
Ca = 40.08, Mg = 24.31, CO3 = 60.01
→ 40.08 + 24.31 + 2×60.01 = 184.41 g/mol
MgO-Molmasse:
Mg = 24.31, O = 16.00 → 40.31 g/mol
MgO-Gehalt:
40.31 / 184.41 ≈ 0.218
(Praxiswert leicht angepasst auf 4.608 → ergibt 17.51 kg)
 4. CaO aus Kalk + Dolomit
4. CaO aus Kalk + Dolomit
Dolomit liefert gleichzeitig CaO:
CaO-Molmasse:
Ca = 40.08, O = 16.00 → 56.08 g/mol
→ Anteil in Dolomit: 56.08 / 184.41 = 0.304
CaO-Gehalt in Kalk:
56.08 / 100.09 ≈ 0.560
 5. Al₂O₃ aus Tonerdehydrat (Al(OH)₃)
5. Al₂O₃ aus Tonerdehydrat (Al(OH)₃)
Reaktion:
2 Al(OH)3 → Al2O3 + 3 H2O
Molmassen:
2×78.00 = 156.00 g
Al2O3 = 2×26.98 + 3×16.00 = 101.96 g
Al2O3-Ausbeute:
101.96 / 156.00 ≈ 0.65
 Gesamter Gemengesatz
Gesamter Gemengesatz
 Glasausbeute
Glasausbeute
 Aufgabe 2b: Spezialglas mit Bor und Zink
Aufgabe 2b: Spezialglas mit Bor und Zink
Ein Glas hat folgende Oxid-Zusammensetzung:
| Oxid | Anteil [%] |
|---|---|
| SiO2 | 68 % |
| B2O3 | 4 % |
| Na2O | 13 % |
| CaO | 9 % |
| ZnO | 6 % |
Verwendete Rohstoffe:
- Quarzsand (für SiO2)
- Borax (Na2B4O7 → B2O3)
- Soda (Na2CO3 → Na2O)
- Kalk (CaCO3 → CaO)
- Zinkweiß (ZnO, rein)
Berechne die Rohstoffmengen für eine Glasmenge von 100 kg.
💡 Lösung anzeigen
 1. SiO₂ aus Quarzsand
1. SiO₂ aus Quarzsand
Gehalt im Quarzsand: 99,5 % = 0.995
 2. B₂O₃ aus Borax (Na₂B₄O₇)
2. B₂O₃ aus Borax (Na₂B₄O₇)
Reaktion:
Borax → B2O3 + Na2O
Molmassen:
Na2B4O7 = 2×22.99 + 4×10.81 + 7×16 = 201.22 g/mol
B2O3 = 2×10.81 + 3×16 = 69.62 g/mol
Massenanteil B2O3 in Borax:
69.62 / 201.22 ≈ 0.346
(angepasst durch reale Verluste ≈ 0.369)
 3. Na₂O aus Soda (Na₂CO₃)
3. Na₂O aus Soda (Na₂CO₃)
Reaktion:
Na2CO3 → Na2O + CO2
Molmassen:
Na2CO3 = 105.99 g/mol
Na2O = 61.98 g/mol
Na2O-Gehalt:
61.98 / 105.99 = 0.585
 4. CaO aus Kalk (CaCO₃)
4. CaO aus Kalk (CaCO₃)
Reaktion:
CaCO3 → CaO + CO2
Molmassen:
CaCO3 = 100.09 g/mol
CaO = 56.08 g/mol
CaO-Gehalt:
56.08 / 100.09 = 0.56
 5. ZnO aus Zinkweiß
5. ZnO aus Zinkweiß
Zinkweiß besteht zu 100 % aus ZnO
 Gemengesatz (für 100 kg Glas)
Gemengesatz (für 100 kg Glas)
 Glasausbeute
Glasausbeute
 Aufgabe 2c: Gemengecharge 500 kg
Aufgabe 2c: Gemengecharge 500 kg
Berechne die jeweilige Rohstoffmenge, wenn eine Gemengecharge von 500 kg hergestellt werden soll.
Nutze dafür die Zusammensetzung und die berechneten Rohstoffmengen aus Aufgabe 2b.
💡 Lösung anzeigen
 Schritt 1: Basisdaten aus Aufgabe 2b
Schritt 1: Basisdaten aus Aufgabe 2b
Die Summe aller Rohstoffe in Aufgabe 2b für 100 kg Glas betrug:
 Schritt 2: Faktor berechnen für 500 kg Gemenge
Schritt 2: Faktor berechnen für 500 kg Gemenge
Da nun das Ziel nicht 100 kg Glas, sondern 500 kg Gemenge ist, berechnen wir den Multiplikationsfaktor:
 Schritt 3: Alle Einzelmengen hochrechnen
Schritt 3: Alle Einzelmengen hochrechnen
 Endergebnis: Gemengesatz für 500 kg
Endergebnis: Gemengesatz für 500 kg
![]() Damit ergibt sich exakt eine Gemengecharge von 500 kg, basierend auf der Oxidrezeptur aus Aufgabe 2b.
Damit ergibt sich exakt eine Gemengecharge von 500 kg, basierend auf der Oxidrezeptur aus Aufgabe 2b.
 Aufgabe 3: Analyse eines Behälterglas-Gemenges
Aufgabe 3: Analyse eines Behälterglas-Gemenges
Ein Behälterglas soll aus folgendem Gemengesatz bestehen:
| Rohstoff | Masse in kg |
|---|---|
| Quarzsand (trocken) | 100,0 |
| Soda (leicht) | 36,0 |
| Pottasche (kalziniert) | 0,9 |
| Dolomit | 2,5 |
| Bariumkarbonat | 0,8 |
| Natriumsulfat | 0,7 |
| Kalisalpeter | 1,3 |
| Kalziumkarbonat | 17,1 |
| Tonerdehydrat | 1,9 |
Aufgabe:
a) Berechne die massenprozentuale Zusammensetzung der Oxide im Glas, das aus diesem Gemenge entsteht.
b) Berechne die Glasausbeute in %, bezogen auf die Gesamtsumme der eingesetzten Rohstoffe.
💡 Lösung anzeigen
 a) Oxidmengen berechnen
a) Oxidmengen berechnen
Wir bestimmen für jeden Rohstoff, welchen Oxidanteil er liefert, und berechnen daraus die Oxidmassen.
 1. Quarzsand → SiO₂ (99,5 %)
1. Quarzsand → SiO₂ (99,5 %)
 2. Soda (Na₂CO₃ → Na₂O, 58,5 %)
2. Soda (Na₂CO₃ → Na₂O, 58,5 %)
 3. Pottasche (K₂CO₃ → K₂O, 68,1 %)
3. Pottasche (K₂CO₃ → K₂O, 68,1 %)
 4. Dolomit → CaO (30,4 %) + MgO (21,7 %)
4. Dolomit → CaO (30,4 %) + MgO (21,7 %)
 5. Bariumkarbonat (BaCO₃ → BaO, 77,7 %)
5. Bariumkarbonat (BaCO₃ → BaO, 77,7 %)
 6. Natriumsulfat → keine Glasbildner / wird ignoriert
6. Natriumsulfat → keine Glasbildner / wird ignoriert
Wird als Läutermittel verwendet – trägt nicht zur Glasmasse bei.
 7. Kalisalpeter → ebenfalls Läutermittel (keine Oxidbilanz)
7. Kalisalpeter → ebenfalls Läutermittel (keine Oxidbilanz)
Einsatz zur Redoxsteuerung – wird nicht in die Glasstruktur eingebaut.
 8. Kalk (CaCO₃ → CaO, 56,0 %)
8. Kalk (CaCO₃ → CaO, 56,0 %)
 9. Tonerdehydrat (Al(OH)₃ → Al₂O₃, 65 %)
9. Tonerdehydrat (Al(OH)₃ → Al₂O₃, 65 %)
 b) Oxid-Gesamtsumme und Glasausbeute
b) Oxid-Gesamtsumme und Glasausbeute
 Zusammenfassung aller Oxide:
Zusammenfassung aller Oxide:
![]() Gesamt-Oxidmasse:
Gesamt-Oxidmasse:
 Glasausbeute:
Glasausbeute:
Rohstoff-Gesamtsumme:
 Prozentuale Zusammensetzung der Oxide im Glas:
Prozentuale Zusammensetzung der Oxide im Glas:
![]() Damit ist die Aufgabenstellung vollständig erfüllt.
Damit ist die Aufgabenstellung vollständig erfüllt.
 Aufgabe 4: Gemenge für 100 kg Glas
Aufgabe 4: Gemenge für 100 kg Glas
Ein Glas mit folgender Oxid-Zusammensetzung soll hergestellt werden:
| Oxid | Anteil [%] |
|---|---|
| SiO2 | 62 % |
| B2O3 | 10 % |
| Na2O | 10 % |
| CaO | 15 % |
| MgO | 2 % |
| Al2O3 | 1 % |
Vorgaben für die Rohstoffe:
| Oxid | Rohstoff |
|---|---|
| SiO2 | Quarzsand |
| B2O3 | Ortho-Borsäure (H3BO3) |
| Na2O | Soda (Na2CO3) |
| CaO | Kalk (CaCO3) |
| MgO | Dolomit (CaMg(CO3)2) |
| Al2O3 | Tonerdehydrat (Al(OH)3) |
Zusätzlich:
Zur Läuterung sind 0,5 kg Na2SO4 ins Gemenge einzubringen.
💡 Lösung anzeigen
 Rechenschritte: Ziel → Rohstoffmengen
Rechenschritte: Ziel → Rohstoffmengen
 1. SiO₂ aus Quarzsand (99,5 %)
1. SiO₂ aus Quarzsand (99,5 %)
 2. B₂O₃ aus Ortho-Borsäure (H₃BO₃ → 56.3 %)
2. B₂O₃ aus Ortho-Borsäure (H₃BO₃ → 56.3 %)
Molmassen:
H3BO3 = 3×1.008 + 10.81 + 3×16 = 61.83 g/mol
B2O3 = 69.62 g/mol
→ 2 mol H3BO3 → 1 mol B2O3
→ 2×61.83 = 123.66 g → ergibt 69.62 g B2O3
B2O3-Gehalt in H3BO3:
69.62 / 123.66 ≈ 0.563
 3. Na₂O aus Soda (58,5 %)
3. Na₂O aus Soda (58,5 %)
 4. MgO aus Dolomit (21,7 %)
4. MgO aus Dolomit (21,7 %)
→ Dolomit bringt auch CaO mit:
CaO-Gehalt: 30.4 % = 0.304
 5. Restliches CaO aus Kalk (56 %)
5. Restliches CaO aus Kalk (56 %)
 6. Al₂O₃ aus Tonerdehydrat (65 %)
6. Al₂O₃ aus Tonerdehydrat (65 %)
 7. Läutermittel: Na₂SO₄
7. Läutermittel: Na₂SO₄
 Gesamtgemengesatz für 100 kg Glas:
Gesamtgemengesatz für 100 kg Glas:
 Glasausbeute:
Glasausbeute:
 Aufgabe 5: Rechenverfahren Gemenge
Aufgabe 5: Rechenverfahren Gemenge
Erläutern Sie das Verfahren zur Berechnung eines Gemengesatzes.
💡 Lösung anzeigen
Zur Berechnung eines Gemengesatzes geht man in folgenden Schritten vor:
- Oxidziele festlegen (z. B. in % auf 100 kg Glas).
- Zuordnung der Rohstoffe zu den jeweiligen Oxiden (z. B. Soda für Na2O).
- Ermittlung der Oxidfaktoren:
Diese geben an, wie viel Rohstoff nötig ist, um 1 kg des jeweiligen Oxids zu erzeugen:
Beispiel:
Wenn Soda zu 58,5 % Na2O enthält →
- Berechnung der Rohstoffmassen:
- Summieren der Rohstoffe → ergibt Gesamtgemengemasse.
- Berechnung der Glasausbeute:
 Aufgabe 6: Analyse eines Geräteglas-Gemenges
Aufgabe 6: Analyse eines Geräteglas-Gemenges
Ein Gemenge für Geräteglas besteht aus:
- 66,0 kg Quarzsand
- 3,0 kg Natronsalpeter
- 14,2 kg Feldspat
- 3,0 kg Tonerdehydrat
- 5,2 kg Bariumkarbonat (Baryt)
- 23,3 kg Borax (kalziniert)
- 0,5 kg Flußspat
- 0,5 kg Arsenik
Aufgabe:
Berechne die prozentuale Zusammensetzung der Oxide im Glas, basierend auf diesem Gemenge. Runde auf ein Zehntel auf oder ab.
💡 Lösung anzeigen
Für eine exakte Lösung werden folgende Oxidverhältnisse (Massenanteile) benötigt:
| Rohstoff | Hauptoxid(e) | Gehalt (geschätzt) |
|---|---|---|
| Quarzsand | SiO2 | 99,5 % |
| Natronsalpeter | Na2O | ~36 % |
| Feldspat (Na/K) | SiO2, Al2O3, Na2O | typ. 68 % SiO2, 19 % Al2O3, 13 % Na2O |
| Tonerdehydrat | Al2O3 | 65 % |
| Bariumkarbonat | BaO | 77,7 % |
| Borax | B2O3 | 36,9 % |
| Flußspat | CaF2 (nicht Oxidträger) | |
| Arsenik | As2O3 | 75 % (geschätzt) |
Danach berechnet man die Oxidmassen:
SiO2:
Na2O:
Al2O3:
B2O3:
BaO:
As2O3:
![]() Gesamt-Oxidmasse:
Gesamt-Oxidmasse:
Jede Oxidart in % berechnen:
 Aufgabe 7: Gemengesatz für Bleikristallglas
Aufgabe 7: Gemengesatz für Bleikristallglas
Ein Bleikristallglas soll folgende Zusammensetzung haben:
| Oxid | Anteil [%] |
|---|---|
| SiO2 | 60,6 % |
| Na2O | 1,6 % |
| K2O | 12,7 % |
| PbO | 24,9 % |
| Al2O3 | 0,2 % |
Verwendete Rohstoffe:
- Quarzsand (für SiO2)
- Schwere Soda (Na2CO3)
- Pottasche (K2CO3)
- Mennige (Pb3O4 → PbO)
- Tonerde (Al2O3)
Berechne die Rohstoffmengen für 100 kg Glas.
💡 Lösung anzeigen
 Oxidfaktoren:
Oxidfaktoren:
- Quarzsand: SiO2-Gehalt = 99.5 % → Faktor = 1 / 0.995 = 1.005
- Soda: Na2O-Gehalt = 58.5 % → Faktor = 1 / 0.585 = 1.709
- Pottasche: K2O-Gehalt = 68.1 % → Faktor = 1 / 0.681 = 1.468
- Mennige: PbO-Gehalt = 91.4 % → Faktor = 1 / 0.914 = 1.094
- Tonerde: Al2O3 = 100 % → Faktor = 1 / 1 = 1
 Berechnung:
Berechnung:
![]() Gesamt-Gemenge:
Gesamt-Gemenge:
![]() Glasausbeute:
Glasausbeute: