Lernkarte 5: Die Phasen der Glasschmelze – Chemie & Physik pur
Lernkarte 5: Die Phasen der Glasschmelze – Chemie & Physik pur
Hallo zusammen! ![]()
Nachdem wir uns die Öfen angesehen haben, schauen wir uns heute an, was in der Wanne eigentlich passiert. Für Industriemeister ist dieses Verständnis essenziell, um Glasfehler (wie Blasen oder Schlieren) richtig zu diagnostizieren.
Der Weg vom sandigen Gemenge zum brillanten Glas unterteilt sich in drei Hauptphasen. Hier ist der Deep-Dive in die Schmelzchemie.
 Der Prozess im Überblick
Der Prozess im Überblick
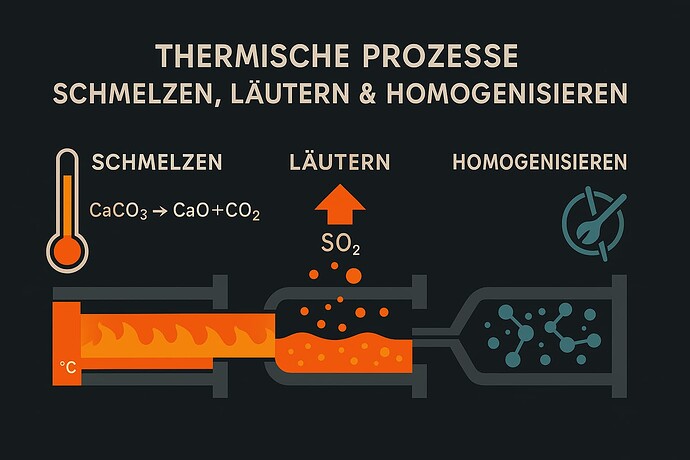
Bevor wir in die Chemie eintauchen, hier der Ablauf als Prozessdiagramm:
 1. Schmelzen (Rauhschmelze)
1. Schmelzen (Rauhschmelze)
Ziel: Aufschmelzen des festen Glasgemenges zu einer viskosen Flüssigkeit.
-
Der Ablauf:
- Das Gemenge wird aufgeheizt \rightarrow Bildung erster Schmelzeinseln (Eutektika), die schwerer schmelzbare Bestandteile (wie Sand/Quarz) langsam auflösen.
- Heftige chemische Reaktionen der Rohstoffe finden statt. Karbonate zerfallen, Kristallwasser verdampft.
- Es entstehen Sinterzonen (Verkleben), Fließzonen und Reaktionszonen.
-
Temperaturen: ca. 1.450 – 1.550 °\text{C}, stark abhängig von Glastyp & Rohstoffen.
-
Wichtige Reaktionen (Dissoziation):
Ein Großteil des Gemengevolumens geht hier als Gas verloren!
(Kalkstein zerfällt zu Calciumoxid und Kohlendioxid)
(Glaubersalz reagiert mit Kohle – wichtig für die Läuterungsvorbereitung)
 2. Läutern (Fining / Entgasen)
2. Läutern (Fining / Entgasen)
Das ist der kritischste Schritt für die Qualität.
Ziel: Entfernung von Gasbläschen (Primärblasen aus dem Gemenge & Sekundärblasen aus Reaktionen) und unerwünschten Einschlüssen.
-
Mechanismen:
- Physikalisches Prinzip: Große Blasen steigen schneller auf als kleine (Gesetz von Stokes).
- Chemisches Prinzip: Läutermittel setzen zusätzlich Gas frei. Dieses Gas diffundiert in die kleinen Blasen, bläht sie auf („Sammelblasen“) und beschleunigt so ihren Aufstieg massiv.
- Thermische Unterstützung: Temperaturerhöhung senkt die Viskosität \rightarrow Blasen steigen leichter auf.
-
Bedingungen:
- Hohe Temperatur (Hot Spot der Wanne).
- Große Oberfläche.
- Lange Verweilzeit.
-
Die Läuter-Reaktionen:
Hier nutzen wir Redox-Reaktionen, die temperaturabhängig Sauerstoff oder Schwefeldioxid abgeben.
Sulfatläuterung (Massenglas):
Antimonläuterung (Spezialglas):
(Bei hohen Temperaturen gibt Sb_2O_5 Sauerstoff ab \rightarrow Blase wächst und steigt auf. Beim Abkühlen nimmt es Sauerstoff wieder auf \rightarrow Restbläschen „kollabieren“ (Resorption).)
 3. Homogenisieren & Abstehen
3. Homogenisieren & Abstehen
Nach dem Läutern ist das Glas zwar blasenfrei, aber chemisch und thermisch noch ungleichmäßig (wie schlecht gerührter Sirup im Wasser).
Ziel: Perfekter Ausgleich von chemischen & thermischen Inhomogenitäten.
-
Störungen bei schlechter Homogenisierung:
- Schlieren: Glasbereiche mit unterschiedlichem Brechungsindex (sichtbare Wellen) oder unterschiedlicher chemischer Zusammensetzung.
- Spannungen: Führen zu Bruch im Kühlofen.
- Farbunterschiede: Ungleichmäßige Verteilung von Farboxiden.
- Lokale Härteunterschiede: Probleme beim Schneiden/Bearbeiten.
-
Maßnahmen:
- Mechanisches Rühren: Rührwerke im Vorherd/Feeder (besonders bei Farbglas).
- Bubbling: Einblasen von Luft am Boden zur Erzeugung einer Walze.
- Temperaturführung: Kontrolliertes Abkühlen („Abstehen“) auf Verarbeitungstemperatur.
- Zeit: Lange Verweilzeiten geben der Diffusion eine Chance.
💡 Merksatz für die Prüfung
„Was nicht schmilzt, wird Stein. Was nicht geläutert wird, bleibt Blase. Was nicht homogenisiert wird, wird Schliere.
Merke: Qualität entsteht in der Wanne, nicht an der Maschine!“
 Community-Frage
Community-Frage
Das Thema Läutermittel ist ja gerade im Wandel. Früher war Arsen (As_2O_3) bei Spezialgläsern Standard, heute wird es aus Umweltgründen vermieden.
Arbeitet ihr noch mit klassischen Läutermitteln oder setzt ihr schon auf rein physikalische Läuterung (z.B. Unterdruck/Vakuum)?
Schreibt es in die Kommentare! ![]()